Cuando era joven, Stephen Crohn vio a sus amigos morir, uno tras otro y sin que él pudiera hacer mucho, de un mal que no tenía nombre.
Cuando su pareja, un gimnasta llamado Jerry Green, cayó gravemente enfermo en 1978 de una enfermedad que ahora conocemos como el síndrome de la inmunodeficiencia adquirida (sida), Crohn simplemente concluyó que él sería el siguiente.
Pero mientras su compañero iba quedándose ciego y exhausto, Crohn permanecía saludable.
Durante la siguiente década, decenas de amigos e incluso otras parejas correrían la misma suerte.
En 1996, el inmunólogo Bill Paxton, quien trabajaba en el Centro de Investigación del Sida Aaron Diamond de Nueva York, buscaba hombres gais que fueran resistentes a la infección, con la intención de descubrir las razones detrás de esa resistencia.
Cuando Paxton trató de infectar los glóbulos blancos de la sangre de Crohn con el VIH en un tubo de ensayo, le resultó imposible.
Lo que pasaba era que Crohn tenía una mutación genética —que ocurre en apenas un 1% de la población— que impide que el virus se adhiera a la superficie de los glóbulos blancos.
Durante los 10 siguientes años, los científicos lograron desarrollar un medicamento retroviral, que imita los efectos de esta mutación en el cuerpo y que logró transformar los tratamientos de esta enfermedad.
El fármaco, además, ha probado ser crucial en ayudar a controlar el virus en personas infectadas.
Aunque Crohn murió en 2013, a los 66 años, su historia deja un legado que va más allá del VIH.
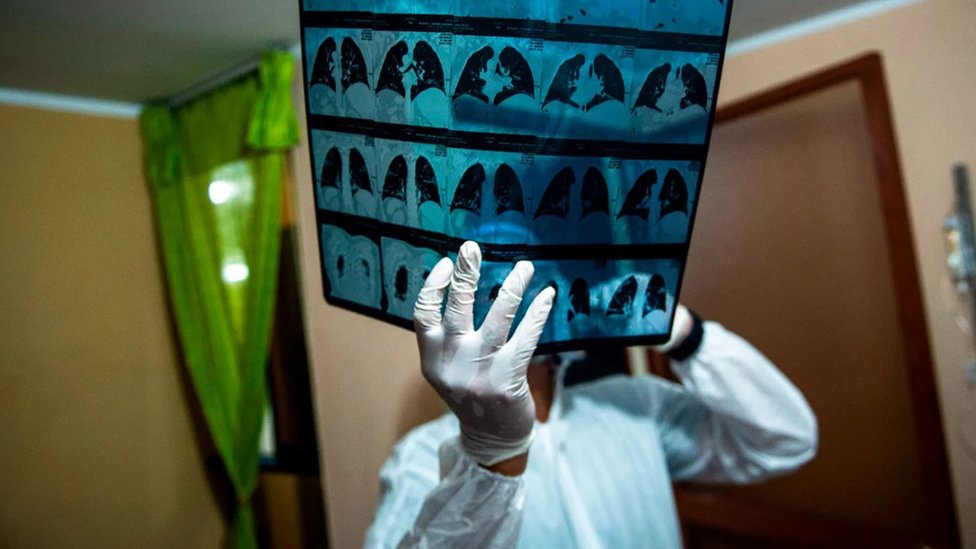
En las últimas dos décadas ha inspirado todo un campo dentro de la medicina, donde los científicos buscan identificar a estos llamados “casos aislados” que, como Crohn, son inusualmente resistentes o poco susceptibles a una enfermedad y son usados como base de estudio de nuevos tratamientos.
Como genetista en la Escuela de Medicina Icahn de Nueva York, Jason Bobe se ha pasado los últimos años dedicado al estudio de personas con rastros de resistencia inusual a enfermedades, desde dolencias cardiacas hasta la enfermedad de Lyme.
Así, cuando la primera ola de covid-19 golpeó el país, su primer instinto fue el de buscar a personas que fueran resistentes a la infección del nuevo coronavirus.
“Pensé en Stephen Crohn. Alguien debía ponerse a buscar esos casos aislados de (resistencia a) la covid-19”, dijo.
La idea de Bobe era tratar de encontrar familias enteras, con varias generaciones, que hubieran sufrido varios casos severos de covid-19 pero entre quienes hubiera un individuo que había resultado asintomático.
“Tener toda una familia junta hace mucho más fácil comprender los factores genéticos que hay en juego, y los que hay detrás de esa resistencia”, explicó.
En el pasado, identificar grupos familiares que cumplieran con estas características habría tomado años, pero el mundo digital ofrece muchas vías de llegada a esas personas.
Desde junio de 2020 Bobe ha estado trabajando con coordinadores de grupos de pacientes de covid-19 y sus familiares en Facebook, como Survivor Corp, para tratar de identificar a candidatos y a sus familias.
También creó una plataforma en internet donde cualquier paciente asintomático de covid-19 puede completar una encuesta para participar en un estudio de resistencia al virus, si es que cumple los requisitos.
En los siguientes meses Bobe espera replicar la secuencia de genomas de pacientes con signos de resistencia a la covid-19, para ver si comparten alguna mutación que les estaría ayudando a evadir el virus.
Si lo logra, sus hallazgos podrían servir de base para la creación de antivirales que nos protejan dela covid-19 y también de futuras epidemias de coronavirus.
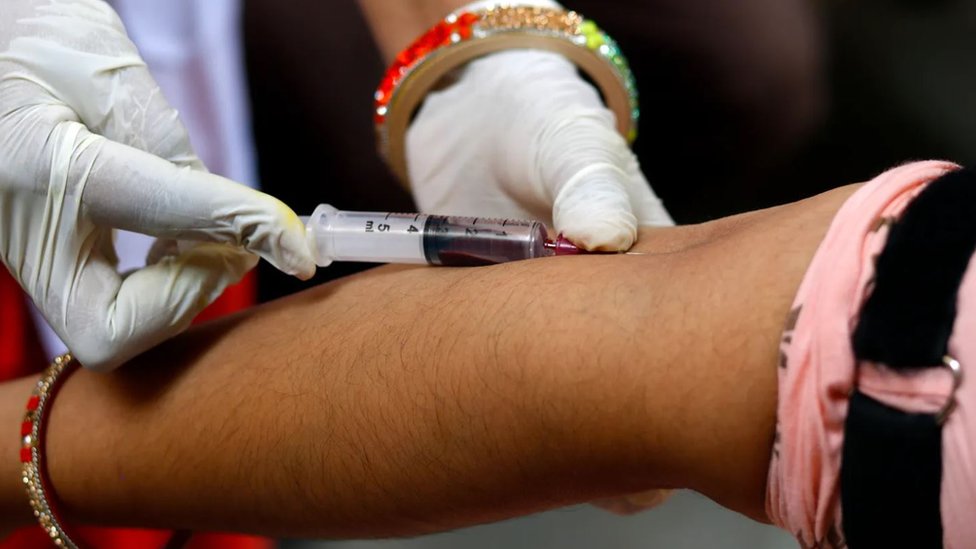
Y ya hay algunas pistas. Los investigadores han identificado una asociación entre el tipo O y los grupos Rh negativos de sangre y un menor riesgo de enfermedad grave.
Pero mientras los científicos señalan en sus hipótesis que ciertos tipos de sangre podría tener naturalmente anticuerpos capaces de reconocer algunos aspectos del virus, la precisa naturaleza de esa relación permanece sin aclararse.

Pero Bobe no es el único científico que intenta dilucidar lo que hace únicos a estos casos aislados de resistencia al covid-19.
Mayana Zatz, directora del Centro de Investigación del Genoma Humano en la Universidad de Sao Paulo, ha identificado a 100 parejas en las que un integrante se contagió de covid-19 y el otro no.
En esta comparación, su equipo está buscando identificar los marcadores genéticos de esa resistencia.
“La idea es tratar de encontrar por qué algunas personas que están muy expuestas al virus no desarrollan covid-19 y, además, no presentan anticuerpos”, señala.
“Descubrimos que, según parece, esto es relativamente común. Recibimos alrededor de 1.000 correos electrónicos de personas que decían que estaban en esta situación”, añade.
Zatz también analizó los genomas de 12 personas mayores de 100 años que apenas resultaron afectadas por el coronavirus, incluyendo una mujer de 114 años en la ciudad de Recife, quien para los registros de Zatz es la persona de más edad que sobrevivió al coronavirus.
Mientras la covid-19 ha resultado especialmente letal entre los adultos mayores, los que han logrado resistir a la enfermedad y son mayores de 70 años pueden ofrecer pistas de nuevas maneras para proteger a los más vulnerables en futuras pandemias.
Mientras los casos de una resistencia notable al virus han llamado la atención de algunos genetistas, otros están más interesados en casos aislados o atípicos del otro extremo del espectro: aquellos afectados en mayor medida que el promedio.

En los últimos meses, estudios de esos pacientes han dado luces sobre por qué el SARS-CoV-2, el virus que causa covid-19, puede llegar a ser tan mortal.
Interrumpir el sistema de alarma del cuerpo
A mediados del año pasado, Qian Zhang llegó a una cita odontológica. En medio de la revisión, el dentista que la atendía le preguntó:
“¿Cómo es posible que yo haya terminado en cuidados intensivos por covid-19, mientras mi hermana se infectó pero casi ni se enteró que estaba contagiada?”.
Como genetista que trabaja en la Universidad Rockefeller de Nueva York, esa era una pregunta que se suponía que Zhang podría responder con facilidad.
En los últimos años, varios científicos de su universidad se han especializado en estudiar el genoma humano para buscar pistas que respondan a por qué hay personas que se enferman gravemente de virus comunes como el herpes o la gripe.
“En todas las enfermedades infecciosas que hemos analizado, siempre se pueden encontrar casos aislados que se enferman de gravedad porque tienen mutaciones genéticas que los vuelven susceptibles”, dice Zhang.
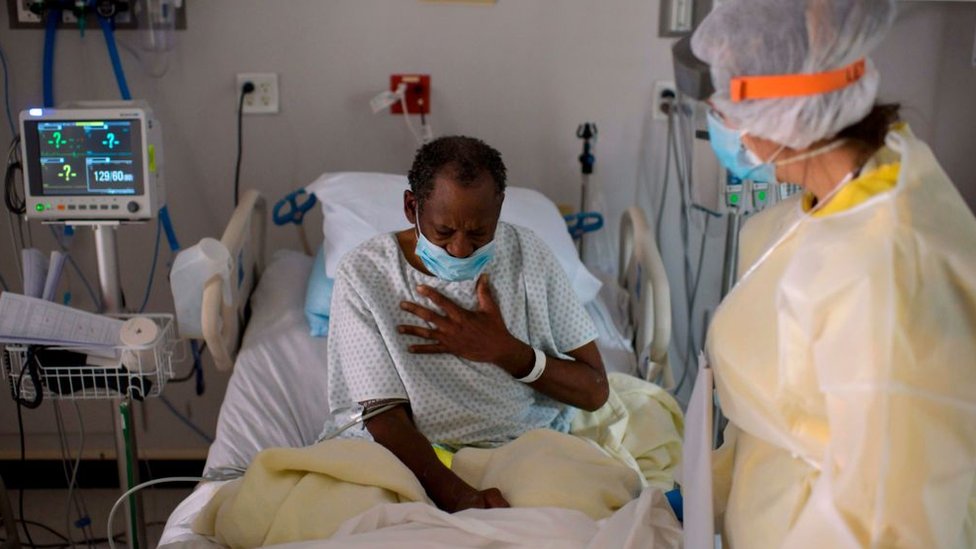
Cuando llegó la pandemia de la covid-19, pronto quedó claro que los adultos mayores, especialmente aquellos con problemas de salud subyacentes, se veían notoriamente afectados, en comparación con la media.
Pero los científicos de Rockefeller estaban más interesados en los casos inusuales de personas aparentemente saludables y de unos 30 años que terminaban en cuidados intensivos.
En abril, lanzaron una colaboración internacional llamada Covid Human Genetic Effort en alianza con otras universidades y centros médicos de Bélgica, Taiwán y otros países, con la idea de estudiar la genética de estos casos.
Apenas comenzado el proyecto, Zhang ya tenía un sospechoso en la mira.
En la década de 1960, los científicos descubrieron que nuestras células tienen un sistema de alarma interno que alerta al resto del cuerpo cuando está siendo atacado por un nuevo virus.
“Cuando un virus entra en una célula, la célula infectada produce proteínas llamadas interferones de tipo uno, que son liberadas fuera de la célula”, explica Zhang.
Y añade: “Todas las células de alrededor reciben esa señal y se dedican a prepararse para combatir ese virus. Si la infección es grave, las células producirán suficiente interferón para que llegue al torrente sanguíneo y de ese modo se entere todo el cuerpo que está siendo atacado”.
Pero algunas veces, hay fallas genéticas que hacen que este sistema no funcione.
En 2015, los científicos del Rockefeller identificaron mutaciones en jóvenes, de otro modo saludables, que llegaron a desarrollar graves casos de neumonía a partir de una simple gripe.
La mutación hacía que no se registrara la respuesta del interferón.
“Si se silencia la alarma, entonces el virus puede propagarse e infectar mucho más rápido”, dice Zhang.
Aparentemente esto ha jugado un rol importante en algunas personas sorpresivamente vulnerables a la covid-19.
Una serie de publicaciones científicas, dadas a conocer en septiembre de 2020, tomó 987 de los llamados casos aislados de covid-19 que habían desarrollado una neumonía severa, pero que eran menores a 50 años o mayores de 50 años sin comorbilidades, y los comparó con pacientes asintomáticos.
Cerca del 3,5% tenía una mutación genética considerable que les impedía generar la respuesta con interferón tipo uno.
Otro 10% tenía un problema con los anticuerpos en la sangre, conocido como autoanticuerpos, que se unen a los interferones y los “sacan” del torrente sanguíneo antes de que puedan alertar al resto del cuerpo.
De acuerdo con Ignacio Sanz, un experto en inmunología de la Universidad de Emory, esto confirma otros hallazgos que sugieren que los autoanticuerpos juegan un papel clave en los casos más severos de covid-19, al bloquear la capacidad del cuerpo de defenderse de los virus.

“Hay evidencia acumulada de que un porcentaje significativo de pacientes con enfermedades graves producen cantidades y tipos inusuales de autoanticuerpos”, explica el experto.
Los científicos de Rockefeller ahora quieren usar esta información para detectar personas que tal vez tengan una vulnerabilidad invisible al covid-19, además de otros virus respiratorios como la gripe.
Zhang explica que cualquier persona con una mutación genética que impida el funcionamiento adecuado de los interferones pueden ser tratada de manera preventiva, o incluso en las primeras etapas de la infección.
“Desde que hicimos el estudio, hemos tenido tres pacientes en París que ya sabían que tenían estas mutaciones genéticas”, explica.
“Después de dar positivo por covid-19, recibieron una inyección de interferón y los tres resultados fueron muy buenos. Sin enfermedad grave”, añade el especialista.
Ellos también están colaborando con bancos de sangre alrededor del mundo para tratar de identificar la verdadera prevalencia en la población general de los autoanticuerpos que actúan en contra del interferón tipo uno.
Si se encuentra que hay un porcentaje significativo, entonces se podría desarrollar un test para determinar si una persona tiene, sin saberlo, un mayor riesgo de contagio frente a las infecciones virales.
“Necesitamos averiguar cuántas personas andan por ahí con estos autoanticuerpos”, dice Zhang.
“Porque muchas de las que participaron en nuestro estudio parecían totalmente sanas y no tenían otros problemas hasta que contrajeron covid-19″, agrega.

Susceptibilidad de los genes
Pero los autoanticuerpos y las mutaciones que bloquean directamente los interferones tipo uno solo representan el 14% de todos estos casos aislados que fueron analizados.
Para el 86% restante, los genetistas creen que la vulnerabilidad se desprende de una serie de cadenas de interacciones genéticas, que los afecta de distintas maneras cuando el virus ataca.
“Solo un pequeño número se infecta gravemente porque tiene una mutación en un único gen principal”, dice Alessandra Renieri, profesora de genética médica en la Universidad de Siena, en Italia.
“La mayoría de los pacientes sigue un modelo más complejo en el que muchos genes cooperan entre sí para aumentar la susceptibilidad ante la covid-19″, añade.
Para poder entender bien esto, científicos de la Universidad de Edimburgo han estudiado los genomas de 2.700 pacientes que se encuentran en unidades de cuidados intensivos en todo Reino Unido y los han comparado con voluntarios sanos.

Y hallaron que la gente más vulnerable a la covid-19 tiene cinco genes —relacionados con la respuesta al interferón y la susceptibilidad a la inflamación pulmonar— que son notoriamente más o menos activos que los de la población general.
“Esta combinación significa que el virus puede propagarse más fácilmente a través de su cuerpo, y tienen más probabilidades de sufrir daño pulmonar como resultado”, explica la genetista Erola Pairo-Castineira, una de los genetistas que dirigieron el estudio.
Pairo-Castineira indica que este conocimiento cambiará el tipo de tratamientos de primera línea que se ofrecen a los pacientes durante futuras pandemias.
En particular, el baricitinib, un antinflamatorio que se usa para tratar la artritis reumatoide, fue identificado por algoritmos de inteligencia artificial como un tratamiento eficaz para el covid-19, en febrero de 2020.
Se sabe que es eficaz para suprimir la actividad de al menos uno de los genes que permiten la inflación de los pulmones.
En diciembre, un ensayo clínico mostró que una combinación de baricitinib y remdesivir antiviral reduce los tiempos de recuperación en pacientes con covid-19.
Tanto los científicos de Rockefeller como los de Edimburgo ahora buscan realizar estudios más amplios de pacientes que han demostrado ser notoriamente susceptibles al covid-19, para hallar más pistas genéticas sobre por qué el virus puede atacar a personas que en apariencia están sanas.
Esto también puede explicar por qué las personas con grupos sanguíneos tipo A parecen tener un factor de riesgo más alto.
El estudio de estos valores aislados de covid-19 también proporciona información sobre otros misterios importantes de la pandemia, como por qué los hombres son marcadamente más susceptibles que las mujeres.
“Estos estudios nos han dado varias ideas al respecto“, dice Renieri. “Nos han demostrado lo importante que es la respuesta del interferón”.
“Esto es interesante porque, después de la pubertad, los hombres experimentan un aumento de testosterona y la testosterona puede regular a la baja los genes del interferón tipo uno. Entonces, para los hombres que ya tienen un defecto en estos genes, significa que podrían ser mucho más vulnerables a los virus”, señala.
Si bien muchas de estas respuestas llegan demasiado tarde para marcar una gran diferencia en la pandemia actual, comprender qué hace que las personas sean particularmente resistentes o vulnerables permitirá salvar muchas vidas durante futuros brotes.
Como nos han demostrado las epidemias de SARS, H1N1 y ébola de los últimos 20 años, es inevitable que nuevos virus continúen propagándose, lo que hace aún más vital el desarrollo de nuevos métodos para identificar a quienes están en mayor riesgo.
Y nuevas formas de tratarlos.
Con esto en mente, el estudio de Zatz sobre adultos mayores resistentes a covid-19 no solo se centra en SARS-CoV-2, sino también en otras infecciones respiratorias.
Su equipo está utilizando células madre para convertir muestras de sangre de estos pacientes centenarios en tejido pulmonar, que luego infectan en el laboratorio con otros múltiples virus para ver si las mutaciones genéticas también ofrecen protección contra estas infecciones.
De ser así, se podría abrir el camino a la producción de medicamentos antivirales completamente nuevos, tal como ocurrió con el estudio de los glóbulos blancos de Stephen Crohn, décadas atrás.
“Nuestro objetivo es identificar variantes genéticas que confieren resistencia, no solo ante el covid-19 sino también ante otros virus o condiciones adversas”, dice Zatz.
“Si identificamos variantes protectoras y descubrimos su función, podríamos abrir nuevas vías de tratamiento”.
